Arbeitsgebiete
Aktivierung und Evolution der Vγ9Vδ2 T-Zellen und die physiologische Bedeutung der Butyrophiline
Die meisten T-Lymphozyten sind MHC-restringierte "konventionelle" T-Zellen. Diese exprimieren einen T-Zell-Antigenrezeptor (TCR), der eine TCR-α und eine β-Ketten (αβTCR) enthält, der Komplexe von (fremden) Peptiden und "antigenpräsentierenden" Zelloberflächenmolekülen, die MHC-Klasse I und II, bindet. Wie auch die antikörperproduzierenden B-Zellen sind diese MHC--restringierten T-Zellen Träger der adaptiven Immunantwort. Die "nicht-konventionellen" T-Zellen exprimieren ebenfalls TCR, zeigen aber auch typische Eigenschaften von Zellen des natürlichen Immunsystems. Sie können sehr schnell aktiviert werden, und ihr TCR erkennt keine pathogen- oder tumorspezifischen Antigene, sondern krankheitsassoziierte molekulare Muster. In vielen Fällen dienen sie nicht (nur) zur Bekämpfung von Krankheitserregern oder Krebszellen, sondern auch zur Kontrolle der Immunantwort oder zur Aufrechterhaltung der Barrierefunktion von Geweben. Wir untersuchen die Mechanismen und Evolution dieser Antigenerkennung und die Aktivierung solcher Zellen.
Nicht-konventionelle T-Zellen umfassen αβ-T-Zellen, die nicht MHC-restringiert sind, sowie die γδ-T-Zellen, die durch ihren TCR definiert sind, der eine γ- und eine δ-Kette enthält. Es gibt zwei Hauptgruppen nicht-konventioneller αβ-T-Zellen, MAIT-Zellen und iNKT-Zellen. Ihr TCR bindet keine Peptid-MHC-Komplexe, sondern Komplexe von MHC-Klasse-I-ähnlichen Molekülen (MR1 oder CD1d) mit Folsäuremetaboliten (MAIT-Zellen) oder (Glyko-)Lipiden. Der γδ-TCR hingegen bindet eine sehr breite Palette strukturell sehr unterschiedlicher Antigene und viele unbekannte Liganden. Wie B-Zellen und αβ-T-Zellen kommen γδ-T-Zellen in fast allen kiefertragenden Wirbeltieren (Kiefermäuler; Gnathostomata) vor.
Eine Besonderheit vieler nicht-konventioneller T-Zellen ist, dass die Nutzung bestimmter TCR-V-Regionen mit ihrer Zellfunktion und Lokalisation korreliert. Dies unterscheidet sich von den TCR der MHC-restringierten αβ-T-Zellen, bei denen eine solche Korrelation nicht besteht und die hauptsächlich in lymphatischen Organen zu finden sind. Ein Beispiel für solche T-Zellen, die durch die TCR-Gene definiert werden, sind die von uns untersuchten Vγ9Vδ2 T-Zellen, deren TCR Vγ9- und Vδ2-genkodierte V-Regionen enthalten. Wie viele nicht-konventionelle αβ-T-Zellen erkennen sie Metabolite mikrobiellen Ursprungs oder Metabolite, die sich in gestressten oder Tumorzellen ansammeln.
1–5 % der peripheren Blut-T-Zellen sind Vγ9Vδ2 T-Zellen. Sie exprimieren Vγ9Vδ2 TCR und erkennen sogenannte Phosphoantigene (PAg), die phosphorylierte Metabolite der Isoprenoidsynthese sind. Vγ9Vδ2 T-Zellen greifen Tumorzellen und Körperzellen an, die mit PAg-produzierenden Krankheitserregern infiziert sind, und breiten sich massiv bei Infektionen wie Malaria oder einigen bakterielle Infektionen aus. Die PAg binden nicht direkt an den Vγ9Vδ2 TCR, sondern müssen von Zelloberflächenmolekülen "präsentiert" werden. Diese Präsentation erfolgt jedoch nicht durch die Bindung des PAg an die extrazelluläre Domäne der MHC-ähnlichen Zelloberflächenmoleküle, sondern durch Bindung an die intrazelluläre Domäne des Zelloberflächenmoleküls BTN3A1. Nach der Bindung an BTN3A1 bildet sich ein aktivierender Komplex mit dem strukturell ähnlichen BTN2A1-Molekül LINK der auch die nicht-PAg-bindenden BTN3-Moleküle BTN3A2 und/oder BTN3A3 enthält. Dieser Komplex wirkt dann als T-Zell-aktivierender Ligand des Vγ9Vδ2 TCR. Die Vγ9Vδ2 T-Zelle erkennt somit Veränderungen der Zelloberflächenproteine, die durch Metabolite innerhalb der Zelle induziert werden.
Phylogenetisch erscheinen Vγ9Vδ2 T-Zellen zusammen mit den plazentalen Säugetieren (Eutheria), sind jedoch während der Evolution bei vielen Spezies wie Mäusen nicht mehr vorhanden, sodass es kein Kleintiermodell für PAg-reaktive Zellen gibt. Wir konnten jedoch zeigen, dass nicht nur Menschen und andere Primaten funktionale Vγ9Vδ2-TCR- und BTN3A-Gene besitzen sondern dass diese auch bei Alpakas (Vicugna pacos) zu finden sind: link. Die Alpaka Vγ9Vδ2-T Zellen reagieren wie die humanen Vγ9Vδ2 T-Zellen auf PAg. Der Vergleich von BTNs und Vγ9Vδ2 TCR beider Arten ermöglichte es uns, Vorhersagen über bestimmte Eigenschaften zu treffen, die für die Funktion dieser Moleküle wesentlich sind. Diese Hypothesen wurden experimentell getestet, indem modifizierte BTN3-Gene in BTN3-defizienten Zellen exprimiert und diese Zellen auf verschiedene Eigenschaften wie die Fähigkeit, Phosphoantigene zu "präsentieren", die Lokalisation von BTN3-Konstrukten in der Zelle, biochemische Eigenschaften und Bildung von Oligomeren sowie die Wechselwirkung mit dem BTN2A1-Molekül analysiert wurden.
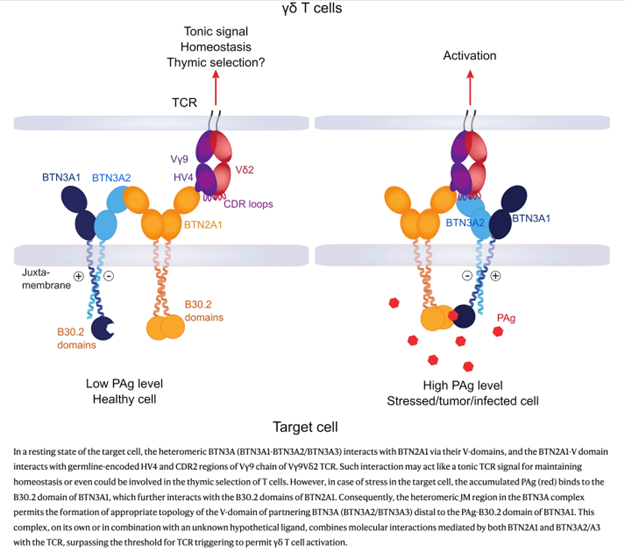
Abbildung aus link Herrmann T, Karunakaran MM. Eur J Immunol. 2024 Nov;54(11):e24510
Diese Experimente führten zu einem neuen Modell der PAg-induzierten Vγ9Vδ2 T-Zellaktivierung. link, die glücklicherweise durch neue CryoEM-Studien zweier chinesischer Gruppen, link link, bestätigt werden.
Wir setzen derzeit die Analysen des Mechanismus der Aktivierung von Vγ9Vδ2 T-Zellen fort, die der Entwicklung einer Vγ9Vδ2 T-zellbasierten Tumortherapie dienen. Ein neues Forschungsfeld ist die Modulation der Immunantwort durch BTN(3)-Moleküle. Hier können wir auf unsere Erfahrungen bei der Analyse der molekularen Basis der BTN-abhängigen Vγ9Vδ2 T-Zellaktivierung zurückgreifen. link